
生体内の運び屋分子『ダイニン』の原子構造を解明
最長のペプチド鎖からなるタンパク質の構造が明らかに
<リリース概要>
大阪大学蛋白質研究所の昆隆英(こんたかひで)准教授と栗栖源嗣(くりすげんじ)教授の研究グループが,細胞内で様々な物質の輸送を駆動するタンパク質分子モーター『ダイニン』の原子構造を決定し,この巨大な分子モーターが長い脚のような構造を使って細胞の中を歩く仕組みの一端を明らかにしました.
ある種の神経変性疾患や不妊・排卵障害の一部はダイニンモーターの機能異常と関連があると考えられています.本研究を基盤としてダイニン運動機構理解が進展すれば,これらダイニン関連病の発症機構が明らかになると期待されます.
<研究の背景>
私たちの体を構成する細胞内では,分子モーターとよばれるタンパク質群が化学エネルギーを力学的運動へと変換することで,生命活動に必要な様々な細胞運動を駆動しています.それらの中で,細胞内物質輸送や繊毛・鞭毛運動を担う『ダイニン』は,分子としての複雑さと分子サイズの巨大さゆえに,主要な分子モーターの中で唯一,全体の立体構造が明らかではなく,その運動機構は謎に包まれていました.
<研究で得られた知見>
図1は,今回,私たちの研究グループが明らかにした細胞性粘菌がもつダイニンモーターの原子分解能での立体構造です。
ダイニンは,ATPを加水分解するリングから長い脚(黄色と橙色)が突き出した構造をもつことが明らかになり,ダイニンがこの脚を構造変化させながら微小管と呼ばれるレールの上を移動することを強く示唆する結果を得ました.また,力発生を担うレバーアーム様の構造(青色)がリングを跨ぐように位置することも可視化され,ダイニンがATP加水分解で得られた化学エネルギーを力学的運動に変換する仕組みについて、原子レベルの構造的知見が得られました.これらの構造的特徴は,従来知られていたミオシンやキネシンという小型分子モーターとは全く異なるものであり,ダイニンは,新しい運動の仕組みによってレール上を運動する分子モーターであることが明らかになりました.
なお,このタンパク質構造は,大型放射光施設SPring8に大阪大学が設置しているビームラインBL-44XUを用いることで得られたもので,これまでに構造決定された最長ポリペプチド鎖のレコードを大幅に更新するものとなりました.この研究成果は,英科学誌Nature誌の発行に先立ち3月8日付け(日本時間)でオンライン版に先行掲載されます.
<研究の波及効果>
ダイニンモーターは,私たちが生きていくうえで欠くことのできないタンパク質分子です.細胞内では,細胞中心方向への輸送のほぼ全てを担っており,さまざまな小胞,細胞内小器官,RNAそしてタンパク質複合体の移動・配置に必須な役割を果たします.また,紡錘体形成や染色体分離など細胞分裂のキープロセスにも深く関与しています.さらに,精子の運動や卵子の輸送を駆動する唯一の分子モーターでもあります.この度の研究結果は,これら生体に重要な細胞運動がどのような仕組みで駆動されているのか,その基本的なメカニズムを明らかにした,重要な研究成果であるといえます.
ダイニンモーターの機能あるいは部分的な機能不全は様々なヒトの疾病と深く関連することが示唆されています.例えば,10種類以上のウィルスが感染過程でダイニン複合体をハイジャックすることが示されています.また, ある種の神経変性疾患や不妊・排卵障害の一部はダイニンモーターの機能異常と関連があると考えられています.本研究を基盤としてダイニン運動機構理解が進展すれば,これらダイニン関連病の発症機構が明らかになると期待されます.
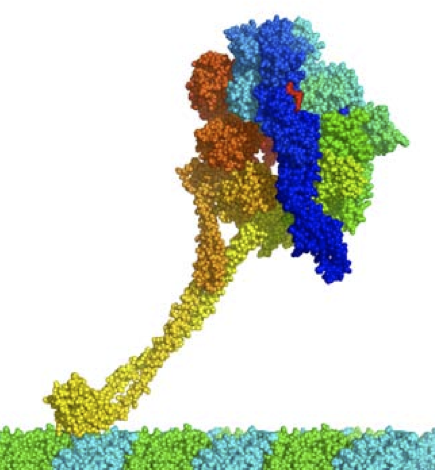
図1:運び屋タンパク質ダイニンの原子構造
